Axit clohidric (HCl) là một trong những hóa chất vô cơ quan trọng và được sử dụng rộng rãi trong nhiều lĩnh vực công nghiệp và đời sống. Với tính axit mạnh, khả năng hòa tan cao và phản ứng nhanh với nhiều kim loại cũng như hợp chất, axit clohidric đóng vai trò không thể thiếu trong các ngành như xử lý nước, luyện kim, sản xuất hóa chất, thực phẩm và tẩy rửa công nghiệp. Tuy nhiên, đi kèm với những ứng dụng đa dạng đó là mức độ ăn mòn và nguy hiểm cao nếu không được sử dụng đúng cách. Bài viết dưới đây sẽ giúp bạn hiểu rõ hơn về đặc điểm, tính chất, ứng dụng cũng như những lưu ý quan trọng khi sử dụng axit clohidric trong thực tế.
Axit Clohidric (HCl) là gì?
Trong cuộc sống hằng ngày cũng như trong nhiều ngành công nghiệp như sản xuất sắt thép, xử lý nước, sản xuất thực phẩm, dược phẩm, hóa chất hữu cơ và vô cơ, xây dựng các chế phẩm, axit clohidric (HCl) được sử dụng rất phổ biến với vai trò là nguyên liệu hoặc chất xúc tác quan trọng.
Axit Clohydric, còn gọi là Hydrochloric acid, là một axit vô cơ mạnh, có tính ăn mòn cao và giữ vai trò quan trọng trong nhiều quy trình hóa học và sản xuất công nghiệp hiện nay.
Khái niệm Axit clohidric HCl
Axit clohidric (ký hiệu HCl) là dung dịch của khí hydro clorua (HCl) hòa tan trong nước.
- Khí hydro clorua (HCl) là một hợp chất vô cơ, ở điều kiện thường tồn tại dưới dạng khí không màu, có mùi hắc, xốc đặc trưng.
- Khi hòa tan vào nước, khí HCl tạo thành dung dịch axit clohydric – một axit mạnh.
Tên gọi khác của HCl:
- Axit hiđrocloric
- Axit muriatic
- Hydrochloric acid
Ở nhiệt độ thường, dung dịch HCl là chất lỏng không màu, trong suốt, đôi khi có màu vàng nhạt nếu lẫn tạp chất.

>>> Xem thêm: Axit Sunfuric (H2SO4)
Các tính chất đặc trưng của Axit clohidric (HCl)
Tính chất vật lý của Axit clohidric (HCl)
Axit clohidric (HCl) tồn tại ở cả dạng khí và dạng dung dịch, mỗi trạng thái có những đặc điểm vật lý riêng biệt.
🔹 Trạng thái và hình dạng
- Dạng khí:
- HCl tồn tại dưới dạng khí hydro clorua, không màu
- Có mùi hắc, xốc, cay, gây ngạt và kích ứng mạnh hệ hô hấp
- Nặng hơn không khí
- Dạng dung dịch (axit clohydric):
- Dung dịch HCl loãng: không màu, trong suốt
- Dung dịch HCl đậm đặc (~40%): có màu vàng ngả xanh lá, dễ tạo sương mù axit, có khả năng ăn mòn mạnh và gây tổn thương nghiêm trọng đến mô người (da, mắt, đường hô hấp)
🔹 Độ tan và tính bay hơi
- Tan rất tốt trong nước, tạo thành dung dịch axit mạnh
- Độ hòa tan trong nước: khoảng 725 g/l ở 20C
- Dung dịch HCl dễ bay hơi, đặc biệt ở nồng độ cao, gây khó khăn cho việc bảo quản và vận chuyển
🔹 Mùi và ảnh hưởng
- Có mùi hắc, cay đặc trưng
- Hơi HCl có thể gây:
- Kích ứng mắt
- Tổn thương đường hô hấp
- Cảm giác bỏng rát khi tiếp xúc trực tiếp
🔹 Các thông số vật lý cơ bản của HCl
- Công thức hóa học: HCl
- Khối lượng mol: 36,5 g/mol
- Độ hòa tan trong nước: 725 g/l (20C)
- Độ nhớt: ~1,80 mPa·s
- Áp suất hơi: ~3,73 Pa
🔹 Nhiệt độ chuyển pha
- HCl khan (dạng khí):
- Điểm nóng chảy: -114,22C
- Điểm sôi: -85,05C
- Dung dịch axit clohydric:
- Điểm sôi thay đổi theo nồng độ
- Dung dịch HCl đậm đặc có điểm sôi khoảng 84C
- Điểm nóng chảy dung dịch khoảng -43C
Tính chất hóa học của Axit clohidric (HCl)
Axit clohidric (HCl) là một axit vô cơ mạnh, có khả năng phản ứng với nhiều chất trong hóa học vô cơ. Các tính chất hóa học của HCl thể hiện rõ tính axit mạnh, tính ăn mòn cao và trong một số phản ứng còn đóng vai trò là chất khử.
- HCl là axit vô cơ mạnh, phân ly hoàn toàn trong nước
- Phản ứng với kim loại hoạt động, oxit bazơ, bazơ và muối của axit yếu hơn
- Có thể thể hiện tính khử khi phản ứng với chất oxi hóa mạnh
- Có tính ăn mòn cao, cần tuân thủ nghiêm ngặt các quy định an toàn khi sử dụng
Tính axit mạnh
- HCl là axit mạnh, phân ly hoàn toàn trong nước:
HCl → H+ + Cl-
- Làm quỳ tím chuyển sang màu đỏ – dấu hiệu nhận biết đặc trưng.
- Ion Cl– là bazơ liên hợp rất yếu, vì vậy việc thêm các muối clorua (NaCl, KCl…) không làm thay đổi pH dung dịch.
Tác dụng với kim loại
Axit HCl phản ứng với các kim loại đứng trước hidro trong dãy hoạt động hóa học (trừ một số trường hợp đặc biệt như Pb do tạo muối ít tan), tạo thành muối clorua và khí hidro.
- Ví dụ với sắt:
Fe + 2HCl → FeCl2 + H2↑
- Ví dụ với nhôm:
2Al + 6HCl → 2AlCl3 + 3H2↑
Lưu ý: HCl không phản ứng với các kim loại đứng sau hidro như Cu, Ag, Au, Hg, Pt…
Tác dụng với oxit kim loại (oxit bazơ)
Axit clohidric phản ứng với oxit kim loại tạo thành muối clorua và nước, trong đó kim loại không thay đổi hóa trị.
CuO + 2HCl → CuCl2 + H2O
ZnO + 2HCl → ZnCl2 + H2O
Tác dụng với bazơ (phản ứng trung hòa)
HCl tác dụng với bazơ tạo thành muối clorua và nước.
NaOH + HCl → NaCl + H2O
Ca(OH)2 + 2HCl → CaCl2 + 2H2O
Al(OH)3 + 3HCl → AlCl3 + 3H2O
Tác dụng với muối
Axit HCl phản ứng với các muối của axit yếu hơn hoặc khi phản ứng tạo ra kết tủa hoặc khí bay hơi, tạo thành muối mới và axit mới.
- Tạo kết tủa:
AgNO3 + HCl → AgCl↓ + HNO3
- Giải phóng khí:
CaCO3 + 2HCl → CaCl2 + CO2↑ + H2O
Na2CO3 + 2HCl → 2NaCl + CO2↑ + H2O
Tính khử của Axit Clohydric
Trong một số phản ứng, HCl thể hiện tính khử khi tác dụng với các chất oxi hóa mạnh, giải phóng khí clo (Cl2).
Các chất oxi hóa thường gặp: KMnO4, K2Cr2O7, MnO2, KClO3.
2HCl + MnO2 → MnCl2 + Cl2↑ + H2O
16HCl + 2KMnO4 → 2KCl + 2MnCl2 + 5Cl2↑ + 8H2O
6HCl + KClO3 → KCl + 3Cl2↑ + 3H2O

Cách điều chế và sản xuất Axit clohidric (HCl)
Axit clohidric (HCl) được điều chế bằng nhiều phương pháp khác nhau, tùy theo quy mô phòng thí nghiệm hay sản xuất công nghiệp. Dưới đây là các phương pháp phổ biến nhất hiện nay.
Điều chế Axit clohidric HCl trong phòng thí nghiệm
Trong phòng thí nghiệm, HCl thường được điều chế bằng phương pháp sunfat, thông qua phản ứng giữa muối natri clorua (NaCl) và axit sunfuric (H2SO4) đậm đặc ở nhiệt độ cao.
Khí HCl sinh ra sau phản ứng được dẫn qua nước để tạo thành dung dịch axit clohydric. Phương pháp này cho HCl có độ tinh khiết cao, có thể đạt nồng độ khoảng 40%.
Phương trình phản ứng:
Ở nhiệt độ dưới 250C:
NaCl (rắn) + H₂SO₄ (đặc) → NaHSO₄ + HCl↑
Ở nhiệt độ trên 400C:
2NaCl (rắn) + H₂SO₄ (đặc) → Na₂SO₄ + 2HCl↑
Axit clohidric điều chế bằng phương pháp này có độ tinh khiết cao, tuy nhiên không được ứng dụng trong sản xuất thương mại do chi phí axit sunfuric cao.
Điều chế Axit clohidric HCl trong công nghiệp
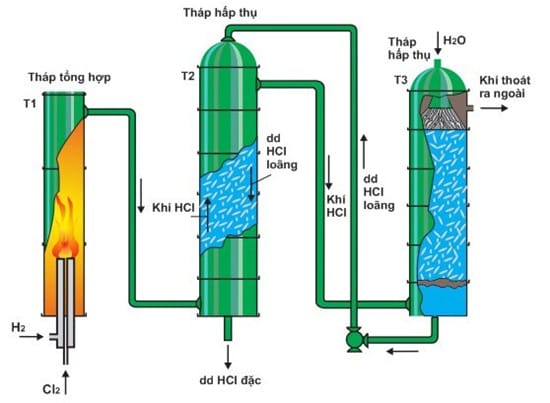
Tổng hợp trực tiếp từ Hydro và Clo
Đây là phương pháp công nghiệp phổ biến nhất để sản xuất HCl có độ tinh khiết cao.
H₂ + Cl₂ → 2HCl (ΔH = -184,74 kJ/mol)
Phản ứng diễn ra trong buồng đốt ở nhiệt độ trên 2000C. Để đảm bảo phản ứng hoàn toàn, người ta cung cấp lượng hydro cao hơn clo khoảng 1–2% nhằm tránh clo dư.
Khí hydro và clo được sản xuất bằng phương pháp điện phân dung dịch NaCl có màng ngăn. Sau phản ứng, khí HCl được hấp thụ vào nước để tạo thành dung dịch axit clohydric.
Sản xuất HCl từ phản ứng với clorua kim loại (phương pháp sunfat)
Quá trình này diễn ra qua hai giai đoạn:
Giai đoạn 1 (150 – 250C):
NaCl + H₂SO₄ (đặc) → NaHSO₄ + HCl↑
Giai đoạn 2 (500 – 600C):
NaCl + NaHSO₄ → Na₂SO₄ + HCl↑
Phản ứng tổng quát:
2NaCl + H₂SO₄ → Na₂SO₄ + 2HCl↑
Khí HCl được lấy ra liên tục nên cân bằng phản ứng dịch chuyển theo chiều tạo sản phẩm. Phương pháp này cho sản phẩm tinh khiết nhưng không phù hợp sản xuất quy mô lớn.
Sản xuất Axit clohidric từ các phản ứng clo hóa hữu cơ (sản phẩm phụ)
Phần lớn axit clohidric công nghiệp hiện nay được thu hồi dưới dạng sản phẩm phụ từ các quá trình clo hóa trong công nghiệp hóa dầu.
Nhiệt phân 1,2-dichloroethan:
C₂H₄ + Cl₂ → C₂H₄Cl₂ C₂H₄Cl₂ → C₂H₃Cl + HCl
Khoảng 90% lượng HCl được sản xuất tại Mỹ thông qua phương pháp này.
Clo hóa ankan:
Cl₂ + RH → RCl + HCl
Phản ứng trao đổi clo với HF:
RCl + HF → RF + HCl
Nhiệt phân chlorodifluoromethane:
2CHF₂Cl → CF₂=CF₂ + 2HCl
Đốt rác thải hữu cơ chứa clo:
C₄H₆Cl₂ + 5O₂ → 4CO₂ + 2H₂O + 2HCl
Tổng hợp Axit clohidric từ hydrat hóa clorua kim loại nặng
Một phản ứng điển hình là hydrat hóa clorua sắt (III):
2FeCl₃ + 6H₂O → Fe₂O₃ + 3H₂O + 6HCl
Khí HCl sinh ra được đưa qua tháp hấp thụ, hấp thụ vào dung dịch axit loãng để tạo thành axit hydrochloric đậm đặc. Dòng khí cuối cùng được xử lý trước khi thải ra môi trường.
Nồng độ Axit clohidric trong sản xuất công nghiệp
- HCl công nghiệp thường có nồng độ từ 30 – 34%
- Dễ vận chuyển, hạn chế bay hơi
- An toàn và kinh tế hơn trong bảo quản và sử dụng
Axit clohidric (HCl) không tác dụng với những chất nào?
Mặc dù là một axit vô cơ mạnh, axit clohidric (HCl) không phản ứng với tất cả các chất. Trong một số trường hợp nhất định, HCl không hoặc hầu như không xảy ra phản ứng hóa học. Dưới đây là các nhóm chất điển hình.
Kim loại đứng sau Hydro (H) trong dãy điện hóa
Axit HCl không phản ứng với các kim loại có tính khử yếu, đứng sau hydro trong dãy điện hóa, bao gồm:
- Đồng (Cu)
- Bạc (Ag)
- Vàng (Au)
- Bạch kim (Pt)
Nguyên nhân: Các kim loại này không thể đẩy hydro ra khỏi dung dịch axit, nên không xảy ra phản ứng với HCl loãng.
Các phi kim
HCl không tác dụng với hầu hết các phi kim trong điều kiện thường, chẳng hạn như:
- Lưu huỳnh (S)
- Photpho (P)
- Cacbon (C)
Do axit clohidric không có tính oxi hóa mạnh, nên không thể phản ứng trực tiếp với các phi kim này.
Các oxit axit (oxit của phi kim)
Axit clohidric không phản ứng với các oxit axit, ví dụ:
- CO2
- SO2
- SO3
- P2O5
- N2O5
Nguyên nhân là do cả HCl và các oxit này đều mang tính axit, nên không xảy ra phản ứng trung hòa.
Một số muối không phản ứng với HCl
HCl không tác dụng với các muối mà phản ứng không tạo ra:
- Kết tủa
- Khí bay hơi
- Chất điện li yếu (như nước)
Ví dụ các muối không phản ứng với HCl:
- NaCl
- KCl
- NaNO3
- KNO3
Lưu ý quan trọng:
Các muối cacbonat (CO32−) và photphat (PO43−) của kim loại kiềm như Na2CO3, K2CO3, Na3PO4, K3PO4 vẫn phản ứng mạnh với HCl, tạo khí CO2 hoặc axit yếu tương ứng.
Ứng dụng của Axit clohidric (HCl) trong công nghiệp và đời sống
Nhờ tính axit mạnh, khả năng phản ứng cao và chi phí hợp lý, axit clohidric (HCl) được ứng dụng rộng rãi trong nhiều lĩnh vực, từ công nghiệp nặng, xử lý nước đến thực phẩm, dược phẩm và đời sống hằng ngày.
Bảng so sánh ứng dụng các nồng độ HCl phổ biến
| Ứng dụng chính | Nồng độ HCl khuyến nghị | Lý do & lưu ý kỹ thuật |
|---|---|---|
| Tẩy gỉ thép (Steel Pickling) | 18% – 32% | Nồng độ cao giúp hòa tan nhanh oxit sắt trước khi cán, mạ hoặc sơn. Cần kiểm soát thời gian và nhiệt độ để tránh ăn mòn thép nền. |
| Xử lý nước & nước thải | <10% hoặc 30–32% (pha loãng) | Dùng để trung hòa pH. Pha loãng giúp kiểm soát pH chính xác, tránh gây sốc hệ vi sinh trong xử lý nước thải. |
| Sản xuất hóa chất & dược phẩm | 32% – 37% | Dùng làm chất xúc tác và thuốc thử trong các phản ứng yêu cầu độ tinh khiết và hiệu suất cao. |
| Phòng thí nghiệm (phân tích) | 37% (PA – tinh khiết) | Yêu cầu nồng độ cao và độ tinh khiết tối đa. Từ dung dịch gốc sẽ pha loãng theo từng thí nghiệm. |
| Công nghiệp thực phẩm | ~10–12% (Food Grade) | Dùng thủy phân protein, điều chỉnh pH. Bắt buộc là loại Food Grade, không chứa kim loại nặng. |
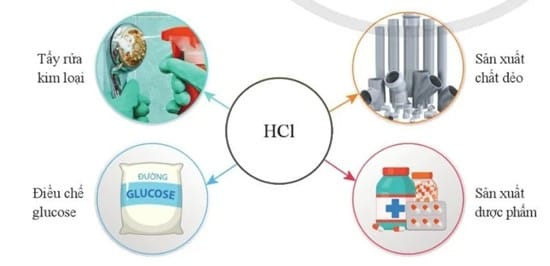
Axit HCl tẩy gỉ thép và làm sạch bề mặt kim loại
Axit clohidric được sử dụng phổ biến để loại bỏ gỉ sét trên bề mặt thép trước khi cán, mạ điện hoặc sơn phủ.
Phản ứng hóa học:
Fe₂O₃ + 6HCl → 2FeCl₃ + 3H₂O
Dung dịch axit sau khi sử dụng có thể được tái sinh và tái sử dụng. Công nghệ pyrohydrolysis cho phép thu hồi HCl theo chu trình khép kín:
4FeCl₂ + 4H₂O + O₂ → 8HCl + 2Fe₂O₃
Sản phẩm phụ Fe₂O₃ được thu hồi và tái sử dụng trong nhiều ngành công nghiệp.

Sản xuất các hợp chất vô cơ bằng axit HCl
HCl là nguyên liệu quan trọng trong sản xuất các muối clorua và hóa chất xử lý nước:
- Sắt(III) clorua (FeCl₃):
Fe₂O₃ + 6HCl → 2FeCl₃ + 3H₂O
- Canxi clorua (CaCl₂):
CaCO₃ + 2HCl → CaCl₂ + CO₂ + H₂O
- Kẽm clorua (ZnCl₂):
Zn + 2HCl → ZnCl₂ + H₂
Các hợp chất này được ứng dụng rộng rãi trong xử lý nước, mạ điện, sản xuất giấy, pin và vật liệu công nghiệp.
Kiểm soát và trung hòa pH bằng axit HCl
Axit clohidric được dùng để điều chỉnh tính bazơ của dung dịch trong xử lý nước và sản xuất công nghiệp:
OH⁻ + HCl → H₂O + Cl⁻
Ứng dụng phổ biến trong xử lý nước thải, hồ bơi, sản xuất thực phẩm và dược phẩm. HCl 32% thường được sử dụng cho hồ bơi do hiệu quả và an toàn.
HCl tái sinh nhựa trao đổi ion và hệ thống lọc nước
Trong công nghệ trao đổi ion, HCl được dùng để tái sinh nhựa trao đổi cation, thay thế các ion Na⁺, Ca²⁺ bằng H⁺, giúp duy trì hiệu suất lọc nước.
Ứng dụng rộng rãi trong hệ thống lọc nước uống, thực phẩm và công nghiệp hóa chất.

Sản xuất các hợp chất hữu cơ
HCl tham gia sản xuất nhiều hợp chất hữu cơ quan trọng như: vinyl clorua, dicloroethane (PVC), polycarbonate, axit ascorbic, than hoạt tính và các dược phẩm.
Ứng dụng trong đời sống và các lĩnh vực khác
- Xử lý nước hồ bơi, diệt khuẩn và tẩy cặn
- Làm sạch gạch, vữa và cặn canxi
- Chế biến da, dệt nhuộm
- Ngành dầu khí (kích thích giếng dầu)
- Pha nước cường toan (HCl + HNO₃) để hòa tan kim loại quý
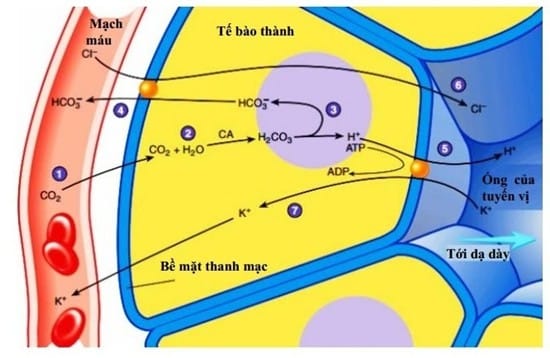
Vai trò sinh học của HCl trong cơ thể người
Trong dạ dày, axit clohidric giúp:
- Tiêu hóa protein
- Tiêu diệt vi khuẩn gây hại
- Kích hoạt enzyme tiêu hóa
- Hỗ trợ hấp thụ vitamin và khoáng chất như Ca, Fe, Zn, Mg
Kết luận: Axit clohidric (HCl) là hóa chất có tính ứng dụng cao, đóng vai trò thiết yếu trong công nghiệp, đời sống và sinh học.
Tác hại của Axit clohidric (HCl) đối với con người và môi trường
Axit clohidric (HCl) là axit mạnh, có tính ăn mòn cao, vì vậy nếu tiếp xúc hoặc sử dụng không đúng cách có thể gây ra nhiều hậu quả nghiêm trọng cho sức khỏe con người và môi trường xung quanh.
Tác hại của khí HCl đối với con người
Việc tiếp xúc trực tiếp hoặc hít phải hơi HCl, đặc biệt trong thời gian dài hoặc ở nồng độ cao, có thể gây ra các ảnh hưởng sau:
- Gây kích ứng mạnh đường hô hấp, dẫn đến:
- Ho dữ dội
- Khó thở
- Viêm phế quản mãn tính
- Đau tức ngực, khàn giọng
- Loét đường hô hấp
- Ảnh hưởng nghiêm trọng đến sức khỏe:
- Nhiễm độc hóa chất
- Viêm dạ dày
- Tổn thương hệ thần kinh trung ương khi phơi nhiễm lâu dài
- Tiếp xúc qua da:
- Gây bỏng hóa chất, tụ máu
- Viêm da, mẩn đỏ
- Hoại tử mô nếu là HCl đậm đặc
- Tiếp xúc với mắt:
- Gây tổn thương giác mạc
- Giảm thị lực
- Có thể dẫn đến mù lòa vĩnh viễn nếu không xử lý kịp thời
- Trường hợp nặng:
- Tích nước ở phổi
- Suy hô hấp
- Nguy hiểm đến tính mạng
Tác hại của HCl đối với môi trường
Khí và dung dịch HCl nếu phát tán ra môi trường sẽ gây nhiều ảnh hưởng tiêu cực:
- Làm cây cối chậm phát triển
- Giảm khả năng quang hợp do:
- Lá cây bị co rút tế bào biểu bì
- Giảm độ “mỡ nóng” trên bề mặt lá
- Ở nồng độ cao:
- Gây cháy lá
- Khô héo
- Thậm chí làm chết cây
- Gây ô nhiễm không khí và đất nếu thải ra môi trường không kiểm soát

Hướng dẫn xử lý sự cố & sơ cứu khi tiếp xúc với HCl
⚠️ Trong các tình huống liên quan đến axit mạnh như HCl, thời gian xử lý quyết định mức độ tổn thương. Cần bình tĩnh và thực hiện đúng quy trình sơ cứu.
Khi HCl dính vào da
- Rửa ngay dưới vòi nước sạch liên tục ít nhất 15–20 phút
- Cởi bỏ toàn bộ quần áo, phụ kiện bị nhiễm axit
Cần đi bệnh viện ngay nếu:
- Vùng bỏng lớn hơn 1 lòng bàn tay
- Da bị phồng rộp, cháy đen hoặc đau dữ dội
- Bỏng ở mặt, mắt hoặc bộ phận sinh dục
👉 Dù vết bỏng nhẹ, vẫn nên đi khám để tránh biến chứng.
Khi HCl bắn vào mắt
- Tuyệt đối không dụi mắt
- Không tự ý nhỏ dung dịch trung hòa
Cách xử lý:
- Rửa mắt dưới nước sạch ít nhất 15 phút
- Mở to mí mắt khi rửa
- Nghiêng đầu để tránh axit lan sang mắt còn lại
- Gọi cấp cứu hoặc đến bệnh viện ngay
Khi hít phải hơi HCl
- Nhanh chóng đưa nạn nhân ra khu vực thoáng khí
- Nới lỏng quần áo
- Để nạn nhân ngồi hoặc nửa nằm để dễ thở
Gọi cấp cứu ngay nếu có các dấu hiệu:
- Ho dữ dội
- Thở gấp, khó thở
- Tím tái, đau ngực
Những lưu ý quan trọng khi sử dụng và bảo quản Axit clohidric (HCl)
Do tính ăn mòn và nguy hiểm cao, khi sử dụng HCl cần tuân thủ nghiêm ngặt các quy định an toàn:
🔹 Bảo hộ cá nhân
- Luôn đeo:
- Găng tay chống hóa chất
- Kính bảo hộ
- Mặt nạ hoặc khẩu trang chuyên dụng
- Quần áo bảo hộ
🔹 Điều kiện làm việc
- Khu vực làm việc phải thông gió tốt
- Tránh làm việc trong không gian kín, thiếu khí
🔹 Lưu trữ và bảo quản
- Lưu trữ tại nơi:
- Khô ráo
- Thoáng mát
- Có thông gió
- Bình chứa phải làm từ vật liệu chống ăn mòn
- Tránh ánh nắng trực tiếp, nguồn nhiệt và độ ẩm cao
🔹 An toàn hóa học
- Không để HCl tiếp xúc với:
- Chất kiềm
- Kim loại dễ phản ứng
- Vật liệu hữu cơ
- Không đổ HCl trực tiếp ra môi trường hoặc cống rãnh
- Tuân thủ đúng quy định xử lý hóa chất nguy hiểm

Xem thêm: máy bơm màng hóa chất
Các loại bơm phù hợp cho Axit HCl
Hydrochloric acid (HCl) là một hóa chất quan trọng và không thể thiếu trong nhiều ngành công nghiệp như sản xuất thép, xử lý nước, dược phẩm, thực phẩm và hóa chất. Tuy nhiên, tính ăn mòn mạnh và độc tính cao của HCl đòi hỏi người sử dụng phải có kiến thức đầy đủ và tuân thủ nghiêm ngặt các biện pháp an toàn.
Để bơm Axit HCl (axit clohydric), cần sử dụng máy bơm hóa chất chuyên dụng với vật liệu có khả năng chống ăn mòn cao như PP, PVDF, ETFE, Inox 316 hoặc Titan. Trong đó, bơm màng và bơm định lượng là những lựa chọn phổ biến nhờ khả năng vận hành an toàn, kiểm soát lưu lượng chính xác và hạn chế rủi ro rò rỉ. Việc lựa chọn đúng vật liệu bơm theo nồng độ và nhiệt độ axit là yếu tố then chốt để đảm bảo độ bền và tuổi thọ thiết bị.
- Bơm định lượng (Dosing Pump): Sử dụng cơ cấu màng hoặc piston, cho phép cấp chính xác lượng axit nhỏ như HCl, H₂SO₄, HNO₃. Thường dùng trong xử lý nước thải, ngành xi mạ, và các hệ thống cần kiểm soát liều lượng chặt chẽ.
- Bơm màng khí nén (AODD – Air Operated Double Diaphragm): Phù hợp với lưu lượng nhỏ đến trung bình, không sử dụng phớt cơ khí, hạn chế tiếp xúc trực tiếp giữa hóa chất và các bộ phận kim loại, đảm bảo an toàn cao.
- Bơm ly tâm hóa chất: Thân bơm và cánh quạt được chế tạo từ PP, PVDF hoặc PTFE, có khả năng kháng axit tốt. Một số dòng bơm trục đứng giúp tiết kiệm không gian lắp đặt.
- Bơm quay tay: Dùng cho nhu cầu bơm thủ công, di chuyển linh hoạt, không cần điện, thân bơm bằng nhựa chịu ăn mòn, phù hợp cho khối lượng nhỏ.
>>> Xem thêm: Khám phá về máy bơm axit HCL
Lưu ý quan trọng khi lựa chọn và vận hành bơm HCL
- Vật liệu bơm: Axit HCl có tính ăn mòn mạnh, cần tránh các kim loại thông thường như nhôm, gang, thép carbon. Nên ưu tiên PP (dưới 40C), PVDF, ETFE, Hastelloy, Titan hoặc Inox 316 cho điều kiện nhiệt độ cao hơn.
- Không vận hành khô: Tuyệt đối không cho bơm chạy khi không có hóa chất, tránh làm hỏng màng bơm, phớt hoặc cánh bơm.
- Nhiệt độ làm việc: Lựa chọn vật liệu phù hợp với nhiệt độ của dung dịch HCl để đảm bảo an toàn và độ bền lâu dài.
- Độ sạch của hóa chất: Axit bơm cần không lẫn cặn bẩn hay tạp chất nhằm bảo vệ các chi tiết bên trong bơm.
- An toàn vận hành: Ưu tiên bơm có phớt kín hoàn toàn hoặc bơm ly tâm không phớt (mag-drive) để hạn chế rò rỉ hóa chất độc hại.

Nguyễn Cường GODO đang làm Digital Marketing GODO Việt Nam kinh nghiệm 10 làm việc trong lĩnh vực máy bơm màng