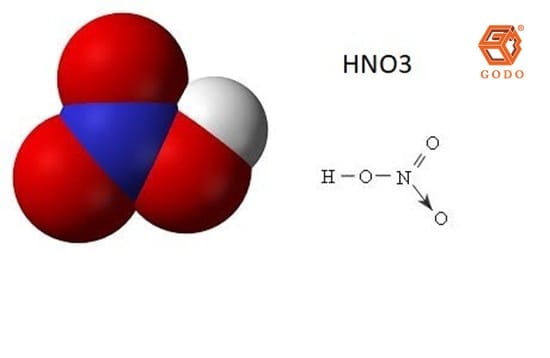
Axit nitric (HNO₃) là một trong những hóa chất vô cơ quan trọng và được sử dụng phổ biến trong nhiều lĩnh vực công nghiệp hiện nay. Với đặc tính axit mạnh, khả năng oxy hóa cao và phản ứng hóa học đa dạng, nitric axit đóng vai trò then chốt trong sản xuất phân bón, thuốc nổ, xử lý bề mặt kim loại, hóa chất công nghiệp và nhiều ứng dụng khác. Tuy nhiên, đi kèm với hiệu quả sử dụng là mức độ ăn mòn và nguy hiểm cao, đòi hỏi người dùng phải hiểu rõ về tính chất, ứng dụng cũng như các biện pháp an toàn khi tiếp xúc. Bài viết dưới đây sẽ giúp bạn tìm hiểu chi tiết về axit nitric, từ đặc điểm, công thức hóa học cho đến các ứng dụng thực tế và lưu ý quan trọng trong quá trình sử dụng.
Axit Nitric (HNO₃) là một trong những axit vô cơ có tính axit mạnh và khả năng oxy hóa rất cao, được sử dụng rộng rãi trong nhiều lĩnh vực của đời sống, đặc biệt là trong sản xuất công nghiệp. Nhờ những tính chất hóa học đặc trưng, HNO₃ đóng vai trò quan trọng trong ngành hóa chất, luyện kim, sản xuất phân bón, thuốc nổ và xử lý bề mặt kim loại.
Vậy axit nitric có những tính chất nổi bật nào, quy trình sản xuất HNO₃ trong thực tế được thực hiện ra sao và ứng dụng cụ thể của hóa chất này là gì? Trong nội dung dưới đây, hãy cùng tìm hiểu chi tiết về axit nitric (HNO₃) để có cái nhìn đầy đủ và chính xác hơn.
Axit Nitric (HNO₃) là gì?
Axit nitric là một hợp chất vô cơ có công thức hóa học HNO₃, còn được gọi là dung dịch nitrat hiđrô hay axit nitric khan. Trong tự nhiên, axit nitric được hình thành từ các cơn mưa giông kèm sấm sét, khi khí nitơ và oxy phản ứng tạo ra các oxit nitơ rồi hòa tan vào nước mưa.
Axit nitric tinh khiết là chất lỏng không màu, có tính bay hơi và bốc khói mạnh trong không khí ẩm. Tuy nhiên, khi để lâu, axit nitric thường chuyển sang màu vàng nhạt do sự tích tụ của các oxit nitơ (NO₂). Đây là một axit mạnh, có tính ăn mòn cao, độc hại và có khả năng gây cháy, nên cần được bảo quản và sử dụng hết sức cẩn trọng.
Những dung dịch có nồng độ axit nitric trên 86% được gọi là axit nitric bốc khói, bao gồm:
- Axit nitric bốc khói trắng
- Axit nitric bốc khói đỏ, tùy thuộc vào lượng NO₂ hòa tan trong dung dịch.
Nhờ các đặc tính hóa học mạnh, axit nitric là một trong những hóa chất được sử dụng rộng rãi trong công nghiệp và đời sống, đặc biệt trong sản xuất phân bón, xử lý kim loại, hóa chất và nhiều lĩnh vực khác.
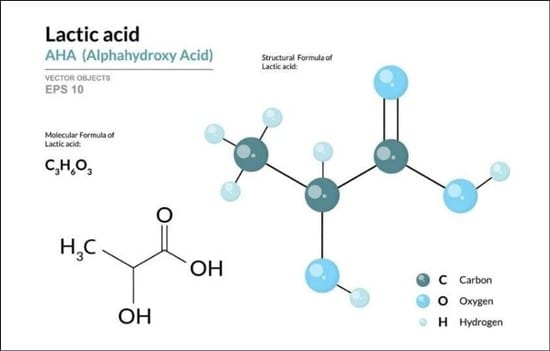
>>> Xem thêm: axit lactic
Tính chất vật lý của Axit Nitric (HNO₃)
Axit nitric là một hợp chất vô cơ mạnh, tồn tại chủ yếu ở dạng chất lỏng không màu, trong một số điều kiện có thể xuất hiện ở dạng khí. Axit nitric tan hoàn toàn trong nước theo mọi tỉ lệ, thường gặp nhất ở nồng độ dưới 65–68%.
Trong điều kiện thường, axit nitric tinh khiết kém bền, dễ bị phân hủy dưới tác dụng của ánh sáng, giải phóng khí nitơ đioxit (NO₂). Khí NO₂ hòa tan trở lại trong dung dịch làm axit nitric có màu vàng nhạt đến vàng đỏ:
4HNO₃ → 4NO₂ + 2H₂O + O₂
Do hiện tượng này, axit nitric cần được bảo quản trong chai lọ tối màu, tránh ánh sáng trực tiếp và nên giữ ở nhiệt độ thấp (dưới 0C) để hạn chế phân hủy.
Axit nitric là chất có tính ăn mòn rất cao, dễ bốc khói trong không khí ẩm, đặc biệt với axit nồng độ cao (khoảng 86%) sẽ xuất hiện hiện tượng khói trắng khi tiếp xúc với không khí. Ngoài ra, HNO₃ là hóa chất cực độc và nguy hiểm, cần tuân thủ nghiêm ngặt các quy định an toàn khi sử dụng.
Một số đặc trưng vật lý quan trọng của axit nitric:
- Tỷ trọng axit nitric tinh khiết: ~1,51 g/cm³ (≈ 1511 kg/m³)
- Tỷ trọng axit nitric 68%: ~1,40 g/cm³
- Nhiệt độ đông đặc: -41C
- Nhiệt độ sôi của HNO₃ tinh khiết: ~83C
Axit nitric có khả năng hòa tan NO₂, tạo dung dịch có màu vàng hoặc đỏ sẫm ở nhiệt độ cao. Hàm lượng NO₂ hòa tan ảnh hưởng rõ rệt đến màu sắc, áp suất hơi và nhiệt độ sôi của dung dịch.
Khi chưng cất hỗn hợp HNO₃ – H₂O, sẽ thu được hỗn hợp đẳng phí (azeotrope) chứa khoảng 68% HNO₃, có nhiệt độ sôi 120,5C tại áp suất 1 atm. Đây cũng là dạng axit nitric đặc phổ biến trong phòng thí nghiệm và công nghiệp.

Tính chất hóa học của Axit Nitric (HNO₃)
Axit nitric (HNO₃) là axit mạnh, monoaxit và chất oxi hóa rất mạnh. Trong dung dịch, HNO₃ điện ly hoàn toàn tạo ion nitrat và ion hiđroni, với hằng số axit rất lớn (pKa ≈ −2).
1. Sự điện ly
HNO₃ là axit monoproton, chỉ phân ly một lần:
HNO₃ + H₂O → H₃O⁺ + NO₃⁻
Do đó dung dịch HNO₃ có tính axit mạnh, làm quỳ tím chuyển sang màu đỏ.
2. Tính chất của axit mạnh
HNO₃ tác dụng với oxit bazơ, bazơ và muối cacbonat tạo thành muối nitrat:
- Với oxit bazơ:
2HNO₃ + CuO → Cu(NO₃)₂ + H₂O - Với bazơ:
2HNO₃ + Mg(OH)₂ → Mg(NO₃)₂ + 2H₂O - Với muối cacbonat:
2HNO₃ + CaCO₃ → Ca(NO₃)₂ + CO₂ + H₂O
3. Tính oxi hóa mạnh của HNO₃
a. Tác dụng với kim loại
Axit nitric phản ứng với hầu hết kim loại, trừ Au và Pt, tạo muối nitrat và sản phẩm khử của N⁺⁵ (NO₂, NO, N₂O, N₂ hoặc NH₄NO₃). Không giải phóng H₂ (trừ một số trường hợp rất loãng, lạnh).
Dạng tổng quát:
M + HNO₃ → M(NO₃)ₙ + H₂O + sản phẩm khử của N
Ví dụ:
- Cu + 4HNO₃ đặc → Cu(NO₃)₂ + 2NO₂ + 2H₂O
- Fe + 4HNO₃ loãng → Fe(NO₃)₃ + NO + 2H₂O
- 8Na + 10HNO₃ → 8NaNO₃ + NH₄NO₃ + 3H₂O
Lưu ý:
- HNO₃ đặc nguội thụ động hóa Al, Fe, Cr do tạo lớp oxit bảo vệ.
- Sản phẩm khử phụ thuộc vào nồng độ axit và tính khử của kim loại:
đặc → NO₂, loãng → NO, rất loãng → mức khử sâu hơn.
b. Tác dụng với phi kim
HNO₃ oxi hóa nhiều phi kim (trừ Si và halogen):
- Với HNO₃ đặc → tạo NO₂
C + 4HNO₃ → CO₂ + 4NO₂ + 2H₂O
P + 5HNO₃ → H₃PO₄ + 5NO₂ + H₂O - Với HNO₃ loãng → tạo NO
3C + 4HNO₃ → 3CO₂ + 4NO + 2H₂O
c. Tác dụng với oxit, bazơ, muối có kim loại chưa đạt hóa trị cao nhất
HNO₃ vừa là axit, vừa là chất oxi hóa:
- FeO + 4HNO₃ → Fe(NO₃)₃ + NO₂ + 2H₂O
- FeCO₃ + 4HNO₃ → Fe(NO₃)₃ + NO₂ + 2H₂O + CO₂
d. Tác dụng với các hợp chất khác
- 3H₂S + 2HNO₃ (>5%) → 3S↓ + 2NO + 4H₂O
- PbS + 8HNO₃ đặc → PbSO₄↓ + 8NO₂ + 4H₂O
- Ag₃PO₄ tan trong HNO₃, HgS không phản ứng với HNO₃.
4. Tác dụng với hợp chất hữu cơ
Axit nitric có khả năng oxi hóa và phá hủy nhiều hợp chất hữu cơ, do đó rất nguy hiểm nếu tiếp xúc trực tiếp với cơ thể người.

Điều chế axit nitric (HNO₃)
Axit nitric trong tự nhiên
Trong tự nhiên, axit nitric được hình thành từ các cơn mưa lớn kèm theo sét. Năng lượng của sét làm cho nitơ và oxy trong không khí phản ứng với nhau, tạo ra các oxit nitơ, sau đó hòa tan trong nước mưa tạo thành axit nitric, gây nên hiện tượng mưa axit.
Điều chế axit nitric trong phòng thí nghiệm
Trong phòng thí nghiệm, axit nitric được điều chế bằng cách cho muối natri nitrat (NaNO₃) tinh thể tác dụng với axit sunfuric đặc (H₂SO₄), sau đó chưng cất hỗn hợp ở nhiệt độ sôi của axit nitric (khoảng 83C) cho đến khi thu được axit nitric và còn lại chất rắn màu trắng.
Phương trình phản ứng:
H₂SO₄ (đặc) + NaNO₃ → HNO₃ + NaHSO₄
Phương pháp này chỉ tạo ra một lượng nhỏ axit nitric, chủ yếu phục vụ cho mục đích nghiên cứu và thí nghiệm.
Axit nitric thu được ban đầu có thể có màu vàng hoặc bốc khói đỏ do lẫn NO₂, sau đó có thể chuyển thành axit nitric màu trắng bằng cách xử lý thích hợp. Khi tiến hành thí nghiệm, dụng cụ phải làm bằng thủy tinh, đặc biệt là bình cổ cong nguyên khối, do axit nitric khan có tính ăn mòn mạnh.
Điều chế axit nitric trong công nghiệp
Trong công nghiệp, axit nitric được sản xuất chủ yếu bằng công nghệ Ostwald, do Wilhelm Ostwald phát minh.
Quy trình gồm các bước chính:
- Oxy hóa amoniac ở nhiệt độ cao (khoảng 850C) với xúc tác platin (Pt):4NH₃ + 5O₂ → 4NO + 6H₂O
- Oxy hóa NO thành NO₂:2NO + O₂ → 2NO₂
- Hấp thụ NO₂ trong nước để tạo HNO₃:4NO₂ + O₂ + 2H₂O → 4HNO₃
Axit nitric thu được thường ở dạng axit loãng, có thể cô đặc đến 68% do tạo hỗn hợp đẳng phí (azeotropic) với 32% nước. Để thu được axit nitric có nồng độ cao hơn, người ta tiến hành chưng cất với axit sunfuric (H₂SO₄), vì H₂SO₄ có khả năng hấp thụ nước mạnh.
Dung dịch axit nitric công nghiệp phổ biến có nồng độ 52% và 68%, được sử dụng rộng rãi trong sản xuất phân bón, thuốc nổ, hóa chất và xử lý bề mặt kim loại.

>>> Xem thêm: Máy bơm hóa chất HNO3 – Giải pháp bơm axit Nitric nồng độ cao
Ứng dụng của Axit Nitric (HNO₃)
Axit nitric (HNO₃) là một axit vô cơ mạnh, có tính oxy hóa cao, được sử dụng rộng rãi trong phòng thí nghiệm và nhiều lĩnh vực công nghiệp quan trọng.
1. Ứng dụng trong phòng thí nghiệm
- Axit nitric được dùng làm thuốc thử liên quan đến ion clorua (Cl⁻). Khi cho HNO₃ tác dụng với mẫu thử rồi thêm dung dịch bạc nitrat (AgNO₃), nếu xuất hiện kết tủa trắng bạc clorua (AgCl) thì chứng tỏ có clorua.
- HNO₃ được sử dụng để điều chế các muối nitrat trong nghiên cứu và phân tích hóa học.
- Axit nitric tinh khiết với nồng độ 0,5 – 2% được dùng làm dung dịch nền trong các kỹ thuật phân tích kim loại vết như ICP-MS và ICP-AES, nhằm xác định sự tồn tại của kim loại trong dung dịch. Việc sử dụng HNO₃ có độ tinh khiết cao là bắt buộc để tránh sai số do ion kim loại tạp.
2. Ứng dụng trong công nghiệp
2.1. Sản xuất thuốc nổ và phân bón
- Axit nitric 68% là nguyên liệu quan trọng trong sản xuất thuốc nổ như:
- Trinitrotoluen (TNT)
- Nitroglycerin
- Cyclotrimethylenetrinitramin (RDX)
- HNO₃ được dùng để sản xuất phân bón chứa nitơ và các muối nitrat như:
- Amoni nitrat (NH₄NO₃)
- Kali nitrat (KNO₃)
- Canxi nitrat (Ca(NO₃)₂)
2.2. Luyện kim, xi mạ và tinh lọc kim loại
- Do phản ứng được với hầu hết kim loại và nhiều hợp chất hữu cơ, axit nitric được ứng dụng rộng rãi trong:
- Ngành luyện kim
- Xi mạ
- Tẩy rửa và tinh lọc kim loại
- Khi kết hợp HNO₃ với axit clohydric (HCl), tạo thành nước cường toan, dung dịch đặc biệt có khả năng hòa tan vàng và bạch kim.
2.3. Sản xuất hóa chất hữu cơ, sơn và thuốc nhuộm
- Axit nitric được dùng để sản xuất:
- Các hợp chất hữu cơ
- Sơn, bột màu
- Thuốc nhuộm vải
- HNO₃ là nguyên liệu để sản xuất nitrobenzen, tiền chất quan trọng trong sản xuất anilin và các dẫn xuất anilin, có vai trò then chốt trong:
- Sản xuất bọt xốp polyuretan
- Sợi aramit
- Dược phẩm
2.4. Sản xuất polyuretan và phụ gia công nghiệp
- Axit nitric là hợp chất trung gian trong sản xuất:
- Bọt xốp polyuretan mềm
- Chất kết dính
- Chất bịt kín
- Chất bọc phủ
- Chất đàn hồi
(từ nguyên liệu toluen diisocyanat)
2.5. Ứng dụng tẩy rửa và xử lý nước
- Trong các nhà máy sữa, HNO₃ được dùng để:
- Tẩy rửa đường ống
- Làm sạch bề mặt kim loại
- Axit nitric giúp loại bỏ tạp chất, cân bằng và điều chỉnh lại chỉ tiêu chất lượng nước trong các hệ thống công nghiệp.
2.6. Ứng dụng đặc biệt khác
- Axit nitric được dùng làm thuốc thử màu (colorimetric test) để phân biệt heroin và morphine.
- Dạng axit nitric không khói trắng (IWFNA) được sử dụng làm chất oxy hóa trong nhiên liệu lỏng cho tên lửa.

An toàn khi tiếp xúc, sử dụng và bảo quản Axit Nitric (HNO₃)
Axit Nitric (HNO₃) là một axit mạnh và chất oxy hóa rất mạnh, có thể phản ứng dữ dội với bột kim loại, hợp chất hữu cơ, nhựa thông và nhiều vật liệu dễ cháy, gây nguy cơ cháy nổ và bỏng hóa chất nghiêm trọng.
Việc hít phải hơi Axit Nitric có thể gây ăn mòn màng nhầy, tổn thương đường hô hấp, phù phổi chậm và trong trường hợp nặng có thể dẫn đến tử vong. Tiếp xúc với mắt có nguy cơ gây tổn thương giác mạc vĩnh viễn, còn nuốt phải sẽ ăn mòn nhanh chóng miệng, cổ họng và đường tiêu hóa.
An toàn khi sử dụng Axit Nitric – HNO₃ 68%
Khi làm việc với HNO₃, người sử dụng cần tuân thủ nghiêm ngặt các quy tắc an toàn:
- Luôn đeo kính bảo hộ hóa chất, tấm chắn mặt, găng tay chịu axit và mặt nạ phòng độc.
- Không để axit tiếp xúc trực tiếp với da.
- Khu vực làm việc phải thoáng khí, có hệ thống thông gió mạnh.
Nếu Axit Nitric văng vào mắt, cần xả liên tục bằng nước sạch trong ít nhất 10 phút và gọi cấp cứu y tế ngay.
Trường hợp tiếp xúc với da, phải xả nước sạch liên tục, cởi bỏ quần áo bị nhiễm hóa chất và rửa bằng dung dịch NaHCO₃ hoặc Na₂CO₃ loãng.
An toàn trong quá trình vận chuyển
Khi vận chuyển Axit Nitric:
- Sử dụng thùng chứa chuyên dụng, đậy kín, tránh rơi vãi hoặc tràn đổ.
- Không vận chuyển chung với kiềm, kim loại hoặc các chất khử.
- Tuyệt đối không dùng mùn cưa, rơm, vỏ bào để thấm hoặc chặn HNO₃ vì có thể gây phản ứng sinh ra khí NO cực độc.
Bảo quản Axit Nitric
Axit Nitric cần được bảo quản trong:
- Khu vực khô ráo, thoáng mát, thông gió tốt.
- Thùng chứa đóng chặt, đậy kín, tránh tiếp xúc với độ ẩm.
- Cách xa chất hữu cơ, kim loại, rượu, kiềm và các chất không tương thích.
👉 Lưu ý quan trọng:
Tất cả các trường hợp tiếp xúc hoặc tai nạn liên quan đến Axit Nitric đều cần được đưa đến cơ sở y tế, để bác sĩ trực tiếp chẩn đoán và xử lý kịp thời, tuyệt đối không tự ý điều trị.
>>> Xem thêm: bơm màng hóa chất
Bơm Axit Nitric (HNO₃) – Lựa chọn bơm và vật liệu phù hợp
Axit Nitric (HNO₃) là axit mạnh, có tính oxy hóa cao và dễ bốc khói, vì vậy việc bơm hóa chất này đòi hỏi phải sử dụng máy bơm hóa chất chuyên dụng với vật liệu kháng ăn mòn cực cao. Tuyệt đối không sử dụng kim loại thông thường, do nguy cơ ăn mòn nhanh, rò rỉ và mất an toàn.
Vật liệu bơm phù hợp để bơm Axit Nitric
- PVDF (Polyvinylidene Fluoride): Lựa chọn tốt nhất để bơm HNO₃, chịu ăn mòn và oxy hóa rất cao, phù hợp với nồng độ đậm đặc.
- PTFE (Teflon): Khả năng kháng hóa chất gần như tuyệt đối, an toàn cho môi trường hóa chất độc hại.
- Nhựa PP: Có thể sử dụng cho một số ứng dụng nhất định, thường áp dụng với nồng độ và nhiệt độ thấp.
- Hạn chế dùng thép không gỉ (inox), chỉ chấp nhận trong trường hợp axit nitric cực loãng và điều kiện làm việc kiểm soát chặt chẽ.
Các loại bơm phù hợp để bơm Axit Nitric
- Bơm màng (Diaphragm Pump)
Bơm màng khí nén phù hợp với axit nitric nồng độ cao, vận hành an toàn do không sử dụng phớt cơ khí, hạn chế rò rỉ. Chịu ăn mòn mạnh, thích hợp cho ngành hóa chất, xử lý nước thải, xi mạ. - Bơm từ tính (Magnetic Driven Pump)
Là bơm ly tâm không phớt, truyền động bằng khớp từ, giúp loại bỏ nguy cơ rò rỉ hóa chất độc hại, phù hợp với hệ thống bơm liên tục. - Bơm thùng phuy (Drum Pump)
Chuyên dùng để hút và chiết axit nitric từ phuy, can, bồn chứa, thường chế tạo từ PVDF hoặc PTFE để đảm bảo an toàn và độ bền.
GODO Việt Nam là nhà cung cấp phân phối dòng sản phầm máy bơm màng chất lượng cao hàng đầu tại Việt Nam với chính sách ưu đãi về giá bán chế độ bảo hành và chất lượng sản phẩm. Sản phẩm bơm màng GODO đang được rất nhiều khách hàng tin dùng trên khắp cả nước. Quý khách có nhu cầu tư vấn lắp đặt bơm màng hãy liên hệ ngay theo số hotline để được tư vấn báo giá chính xác nhất.

Nguyễn Cường GODO đang làm Digital Marketing GODO Việt Nam kinh nghiệm 10 làm việc trong lĩnh vực máy bơm màng